Los aldehídos y cetonas pueden ser preparados por oxidación de alcoholes, ozonólisis de alquenos, hidratación de alquinos y acilación de Friedel-Crafts como métodos de mayor importancia.
a) Ozonólisis de alquenos: Los alquenos rompen con ozono formando aldehídos y/o cetonas. Si el alqueno tiene hidrógenos vinílicos da aldehídos. Si tiene dos cadenas carbonadas forma cetonas.
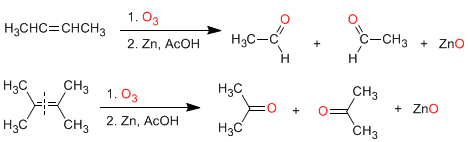
a) Ozonólisis de alquenos: Los alquenos rompen con ozono formando aldehídos y/o cetonas. Si el alqueno tiene hidrógenos vinílicos da aldehídos. Si tiene dos cadenas carbonadas forma cetonas.

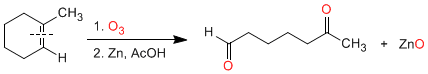
La ozonólisis de alquenos cíclicos produce compuestos dicarbonílicos:
Los alquenos terminales rompen formando metanal, que separa fácilmente de la mezcla por su bajo punto de ebullición.
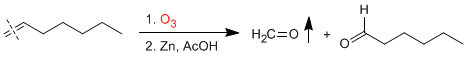
b) Oxidación de alcoholes: Los alcoholes primarios y secundarios se oxidan para dar aldehídos y cetonas respectivamente. Deben tomarse precauciones en la oxidación de alcoholes primarios, puesto que sobreoxidan a ácidos carboxílicos en presencia de oxidantes que contengan agua. En estos caso debe trabajarse con reactivos anhídros, como el clorocromato de piridino en diclorometano (PCC), a temperatura ambiente.
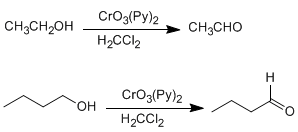
Los alcoholes secundarios dan cetonas por oxidación. Se emplean como oxidantes permanganato, dicromato, trióxido de cromo.
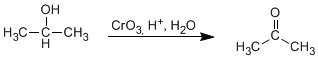
La oxidación supone la pérdida de dos hidrógenos del alcohol. Los alcoholes terciarios no pueden oxidar puesto que carecen de hidrógeno sobre el carbono.
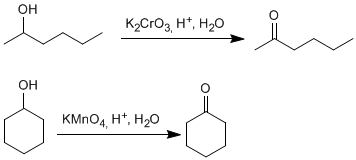
Los alcoholes alílicos y bencílicos se transforman en aldehídos o cetonas por oxidación con dióxido de manganeso en acetona. Esta reacción tiene una elevada selectividad y no oxida alcoholes que no se encuentren en dichas posiciones.
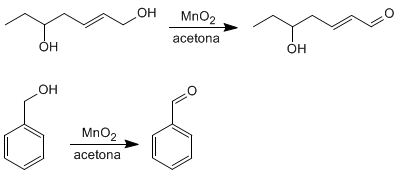
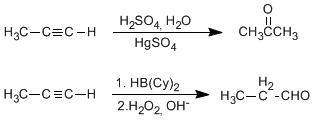
c) Hidratación de alquinos: Los alquinos se pueden hidratar Markovnikov, formando cetonas, o bien antiMarkovnivov, para formar aldehídos.
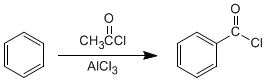
d) Acilación de Friedel-Crafts: La introducción de grupos acilo en el benceno permite la preparación de cetonas con cadenas aromáticas.
VÍDEO:
Comentarios
Publicar un comentario